8 月 30 日~9 月 2 日,2024 年欧洲心脏病学会年会(ESC 2024)在英国伦敦召开。今年大会的主题是「个性化心血管护理」,聚焦疾病发展的各个阶段,通过个性化治疗降低风险,改善患者预后。本次 ESC 可谓是一场学术盛宴,诸多最新研究成果发布。本期我们聚焦转甲状腺素蛋白心脏淀粉样变心肌病(ATTR-CM)领域,进行全新视角解读。
ATTR-CM 作为一种「孤儿病」正逐渐获得更多的关注
ATTR-CM 是一种由不稳定的转甲状腺素蛋白(TTR)四聚体解离成单体后错误折叠,最终以淀粉样物质沉积于心肌间质而引发的浸润性心肌病。2018 年,ATTR-CM 作为特发性心肌病的一种,被列入了 121 种罕见病名录[1]。然而,尽管 ATTR-CM 被视为一种罕见病,但近年来相关研究表明,其真实的发病率可能被严重低估。根据最新公布的流行病学调查数据,2004 至 2021 年间,英国每 10 万人中的 ATTR-CM 发病率已经从 0.75 上升至 1.96,新确诊患者数量更是增加了 2.9 倍[2]。
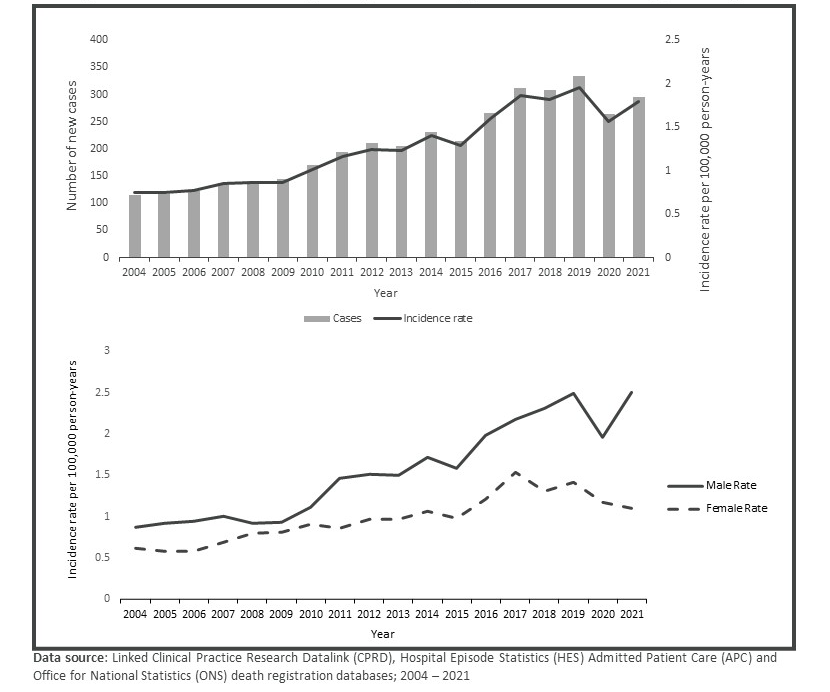
图 1 英国人群 ATTR-CM 发病率(2004~2021)
随着 ATTR-CM 发病率的逐年攀升,这种疾病正引起越来越多的关注。面对这一趋势,亟需加快建立规范化的管理流程,以推动诊断技术的进步,同时加速药物的迭代更新,从而有效改善患者的预后。随着医疗技术的发展,特别是在诊断和治疗领域的持续创新,我们有理由期待,ATTR-CM 患者将在未来获得更早的诊断和更加精准的治疗,进而提升生活质量并延长生命。
心脏受累为 ATTR-CM 显著的临床表现
在多种因素的影响下,不稳定的三级结构蛋白质可能发生错误折叠并聚集,形成淀粉样物质,最终沉积在心脏、肾脏、肝脏、肺以及其他器官中,导致多个组织的损伤和器官功能障碍[3]。ESC 大会上发布的多国研究数据进一步强调了心脏表现作为最常见的前驱症状的重要性。OverTTuRe 研究是一项在美国和日本开展的跨国研究[4],纳入了年龄 ≥ 18 岁并确诊为 ATTR-CM 或接受过 ATTR 特异性治疗的患者。研究结果显示,在确诊为 ATTR-CM 的前 5 年内,心力衰竭是最常见的临床表现(美国:30.3%;日本:42.0%),其次是房颤(21.9%,美国)和心肌病(21.7%,美国)。这一研究提示临床医师需高度重视早期出现心脏表现的患者,以便及时识别并干预,防止疾病的进一步恶化。这项研究的结果为临床实践提供了宝贵的指导,强调了在早期阶段关注心脏症状的重要性,有助于提高 ATTR-CM 的早期诊断率,并为患者提供更早的治疗干预,从而改善预后。
诊断工具逐渐多样化,早期诊断成为可能
由于对 ATTR-CM 的认识不足、临床表现缺乏特异性等原因,ATTR-CM 误诊率高、诊断延迟。2024 ESC 大会公布了一项在德国进行的真实世界研究[5],该研究评估了 ATTR-CM 患者的诊断和治疗的延误情况。结果显示,从最初怀疑 ATTR-CM 到最终确诊,平均时间为 300 天。由此可知,ATTR-CM 诊断延迟的问题十分严峻。
随着经济和科技的飞速发展,越来越多的诊断工具被开发出来,其中人工智能(AI)在医疗领域的应用尤为引人注目。大会公布了一项前沿研究[6],评估了 AI 算法在心电图(ECG)图像和超声心动图分析中的应用效果,以便更早、更准确地诊断 ATTR-CM。该研究共纳入了 234 例 ATTR-CM 患者,患者随机采用 AI ECG 或 AI 超声心电图进行诊断。结果显示,在确诊前的 1 至 3 年间,通过 AI 分析 ECG 和超声心动图筛查出阳性患者比例分别为 52.4% 和 34.7%。这一比例在确诊前的 12 个月内显著提升,分别达到了 75.6% 和 69.4%。这表明,AI 技术不仅能够有效识别出早期甚至亚临床阶段的 ATTR-CM 患者,还为早期干预提供了新的可能性,从而有助于防止疾病进一步进展,改善患者的预后。这项研究充分展示了 AI 在医学诊断领域的巨大潜力,表明在临床实践中引入 AI 技术,能够显著提高复杂疾病的早期检测率,为患者提供更为及时和有效的治疗。
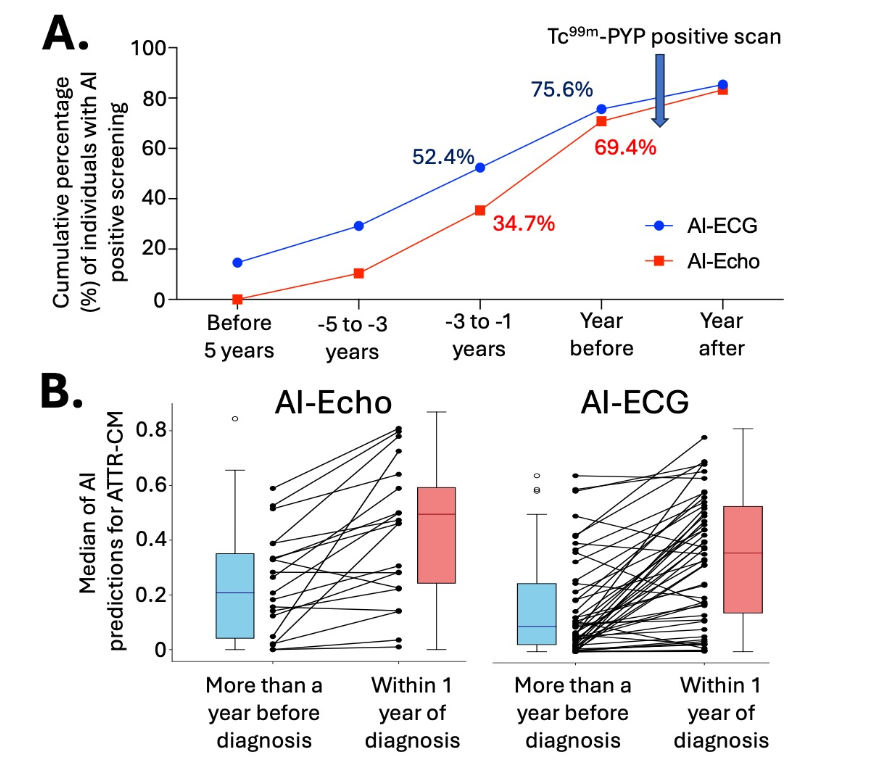
图 2 A:AI 筛查阳性率(%);B:ATTR-CM 预测情况
ATTR-CM 治疗领域再添新证
针对 ATTR-CM 的治疗策略通常分为对症治疗和病因治疗,而靶向治疗则包括抑制 TTR 蛋白合成和稳定 TTR 蛋白的药物。其中,Vutrisiran 作为一种 RNA 干扰(RNAi)药物,通过靶向 TTR mRNA,从根本上抑制 TTR 蛋白的产生,从而减少在周围神经中的淀粉样沉积,避免组织和器官的损伤,真正从病因上解决 ATTR 淀粉样变性问题。
大会上公布的 HELIOS-B 三期临床试验[7]的结果进一步证实了 Vutrisiran 的疗效。该研究纳入了来自 26 个国家的 87 个中心的 655 例患者,这些患者被随机分为两组,每三个月接受一次 25 毫克的 Vutrisiran(n = 326)或安慰剂(n = 329),治疗时间最长可达 36 个月。试验结果显示,与安慰剂组相比,Vutrisiran 治疗组显著降低了全因死亡率和复发性心血管事件的风险。在总体人群(总体患者,655 例)中,Vutrisiran 的风险比为 0.72(95% CI 0.56~0.93;P = 0.01),而在单药治疗人群(vutrisiran 组中 196 例(60%)和安慰剂组中 199 例(60%)在基线时未服用 tafamidis,这些患者构成了单药治疗人群)中,其风险比为 0.67(95% CI 0.49~0.93;P = 0.02)。这一数据表明,Vutrisiran 不仅能够有效减缓疾病的进展,还能显著降低患者的死亡和心血管事件风险,为 ATTR-CM 患者提供了更为有力的治疗选择。
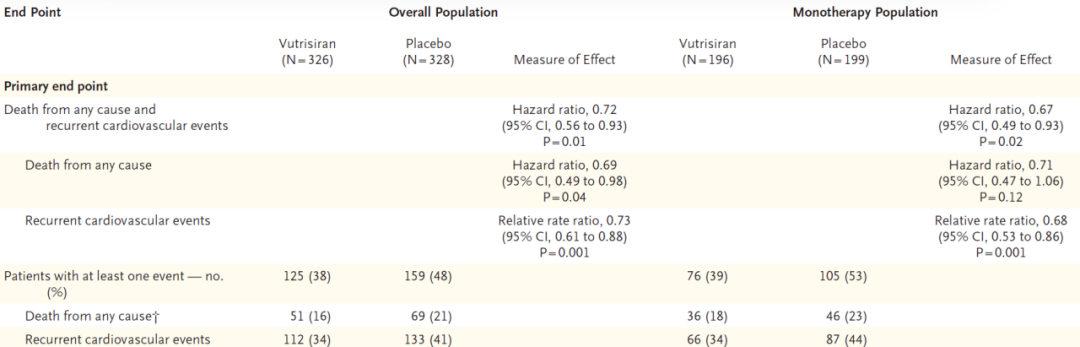
图 3 主要终点结果分析
自 2018 年 FDA 批准第一款 siRNA 药物上市,小核酸药物迎来了发展的新纪元,大会公布的 HELIOS-B 三期临床数据更是为 siRNA 药物的应用提供了更为有力的证据。同样是小核酸药物的 Eplontersen 也展现出了较好的疗效,其与 Vutrisiran 作用靶点相同。2023 年公布的最新数据表明,Eplontersen 能够使血清 TTR 浓度从基线上平均减少 81.7%[8],具有较好的疗效,已于 2023 年底获得 FDA 审批。Eplontersen 是首个可以通过自动注射器自行给药的治疗 ATTR-CM 药物,具有更好的便捷性,在临床中逐步推广应用,将使更多患者获益。
小结
近年来,随着对 ATTR-CM 认识的不断加深以及诊断技术的日益进步,ATTR-CM 的确诊率逐渐上升,凸显出这一疾病的重要性和紧迫性。早期诊断和早期干预已成为改善患者预后的关键。在这一背景下,AI 算法的应用展现出了显著的优势,不仅能有效缩短 ATTR-CM 的诊断时间,还具备高度的敏感性,未来有望在临床中广泛推广,助力于更早地发现疾病,从而为及时治疗争取宝贵的时间。
在治疗领域,越来越多的创新药物不断涌现,其中,Vutrisiran 因其卓越的疗效而备受瞩目。HELIOS-B 三期临床试验的最新结果进一步证实了 Vutrisiran 在治疗 ATTR-CM 中的显著优势,为其临床应用提供了坚实的证据。同样作为小核酸药物的 Eplontersen 也展现出了较好的疗效。ATTR-CM 治疗领域药物正「朝气蓬勃」的发展,相信随着 Vutrisiran、Eplontersen 等药物的逐步推广应用,ATTR-CM 患者将有望获得更好的预后和更高的生活质量。
未经允许不得转载:澳鸟-全球资讯平台 » 2024 ESC:聚焦转甲状腺素蛋白心脏淀粉样变性,全新视角解读

 澳鸟-全球资讯平台
澳鸟-全球资讯平台









